Johdanto
Solususpensioviljelyteknologiasta on tullut modernin biolääketieteellisen tuotannon kulmakivi. Varhaisesta käytöstä rokotteiden kehittämisessä aina laajamittaiseen terapeuttisten vasta-aineiden valmistukseen asti tämä teknologia on mullistanut biologisten tuotteiden tuotannon tehokkuuden, skaalautuvuuden ja turvallisuuden. Tässä artikkelissa esitetään suspensioviljelyteknologian kehityshistoria, nykytila ja keskeiset tekniset komponentit sekä korostetaan sen tulevaisuudennäkymiä, erityisesti rokotteiden tuotannon alalla.
Suspensioviljelyteknologian historiallinen kehitys
Laajamittainen soluviljely alkoi vuonna 1962, kun Capstick ym. sovelsivat BHK-21-soluja suspensioviljelyyn eläinrokotteiden tuottamiseksi. Tämä innovaatio loi pohjan teolliselle solupohjaiselle rokotetuotannolle. Vuonna 1967 Van Wezelin mikrokantajien käyttöönotto mahdollisti kiinnittyneiden solujen viljelyn bioreaktoreissa, mikä laajensi entisestään skaalautuvan tuotannon laajuutta.
1980-luvulle mennessä CHO-solujen (kiinanhamsterin munasarjasolut) käyttö suspensioviljelmissä ja monoklonaalisten vasta-aineiden teknologian kehitys katalysoivat bioreaktorien laajaa käyttöönottoa biolääketeollisuudessa. 2000-luvun vaihde toi mukanaan lisää teknologisia innovaatioita, kuten virtaussyöttöisiä ja perfuusioviljelyjärjestelmiä sekä räätälöityjä viljelyalustoja, mikä johti suurten tilavuuksien, yksinkertaistettujen ja skaalautuvien bioreaktorijärjestelmien syntymiseen. Nykyään yli 100 bioreaktoria maailmanlaajuisesti ylittää 10 000 litraa, ja suurin on 25 000 litraa. Näitä käyttävät pääasiassa johtavat yritykset, kuten Genentech, Amgen, Boehringer Ingelheim ja Lonza.
Nykyinen tila ja maailmanlaajuinen soveltaminen
Suspensioviljelystä on tullut biolääketieteellisten lääkkeiden tuotannon valtavirtateknologia. Nykyaikaiset prosessit sisältävät tyypillisesti seerumittomia elatusaineita ja kontrolloidusti virtaussyöttöistä viljelyä mekaanisesti sekoitetuissa bioreaktoreissa. Vuonna 2007 viisi kuudesta myydyimmästä biolääketieteellisestä tuotteesta tuotettiin nisäkässolujen ilmentämisjärjestelmillä.
Tällä teknologialla on erityinen vaikutus rokotetuotannossa. Esimerkiksi MDCK-soluja käytetään nyt suspensioviljelmissä influenssarokotteiden valmistukseen, mikä korvaa perinteiset kananmunaan perustuvat tuotantomenetelmät. 10 litran suspensioviljelmällä voidaan saavuttaa 10 000 kanan alkiota vastaava virustuotanto. Yritykset, kuten Baxter, Crucell, Sanofi Pasteur ja Novartis, ovat kehittäneet omia solualustojaan – kuten Vero-, PER.C6- ja MDCK-solulinjoja – jotka on räätälöity teollisen mittakaavan rokotetuotantoon.
Keskeiset teknologiat suspensioviljelyprosesseissa
- Solulinjan kehitys ja kesyttäminen
- Viruksen herkkyys ja sopeutuminen
- Räätälöidyt viljelyalustat
- Prosessien kehittäminen ja optimointi
1. Solulinjan kehitys ja kesyttäminen
Menestyksekäs laajamittainen tuotanto perustuu solulinjoihin, joilla on korkea saanto, vakaa ilmentyminen ja virusherkkyys. Domestication-prosessiin kuuluu sellaisten solujen seulonta, sopeuttaminen ja säilöminen, jotka kykenevät kasvamaan tiheästi, seerumittomassa muodossa tai suspensiossa samalla, kun säilytetään korkea elinkelpoisuus ja tuottavuus. Yritykset, kuten Lonza ja Novartis, ovat kehittäneet erikoistuneita solulinjoja transfektion ja klooniseulonnan avulla parantaakseen saantoa moninkertaisesti.
2. Viruksen herkkyys ja sopeutuminen
Virusten yhteensopivuus isäntäsolujen kanssa on ratkaisevan tärkeää. Viruskannat vaativat usein sopeutumista lisääntyäkseen tehokkaasti suspensioviljelmissä. Esimerkiksi aiemmin alkioissa viljeltyjä rabiesviruskantoja on sopeutettu Vero- ja BHK-21-soluihin reaktoripohjaista suspensiotuotantoa varten.
3. Räätälöidyt viljelyalustat
Elatusalustan koostumus on kriittisin tekijä soluviljelyn onnistumisessa. Optimoidut, kemiallisesti määritellyt elatusaineet voivat parantaa merkittävästi proteiinien ilmentymistä ja varmistaa yhdenmukaisuuden. Vaikka maailmanlaajuiset valmistajat käyttävät rutiininomaisesti räätälöityjä elatusaineita, jotka on kehitetty yhteistyössä erikoistuneiden toimittajien kanssa, Kiina luottaa edelleen pääasiassa vanhentuneisiin luetteloformulaatioihin, kuten MEM ja RPMI1640, mikä korostaa modernisoinnin tarvetta.
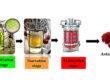
4. Prosessien kehittäminen ja optimointi
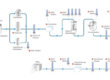
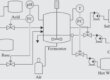
Suspensioviljely voidaan toteuttaa panos-, virtaussyöttö- tai perfuusiomenetelmillä. Jokaisella on omat vahvuutensa solutyypistä ja tuotteesta riippuen. Esimerkiksi perfuusioviljely on ihanteellinen lyhyen puoliintumisajan omaavien erittyvien proteiinien tuottamiseen, kun taas virtaussyöttöjärjestelmät tarjoavat korkean saannon ja yksinkertaisen käytön. Reaktoriprosessin hallinta – mukaan lukien lämpötila, pH, liuennut happi ja osmoottinen paine – on välttämätöntä optimaalisten kasvuolosuhteiden ylläpitämiseksi.
Bioreaktorien valinta ja skaalaus
Skaalattavat, mekaanisesti sekoitetut reaktorit ovat alan standardi suspensioviljelylle. Suuritilavuuksiset reaktorit vähentävät infrastruktuuri- ja työvoimakustannuksia verrattuna useiden pienempien yksiköiden käyttöön. Laitteiden valinnassa tulisi ottaa huomioon tuotantomittakaava, prosessien yhteensopivuus, rajapintojen standardointi ja toimittajien tuki luotettavuuden ja toiminnan tehokkuuden varmistamiseksi.
Tulevaisuudennäkymät
Teknologian kypsyessä odotetaan laajempaa soveltamista ja standardointia biolääketieteen alalla. Perimmäinen tavoite ulottuu kuitenkin tuotantolinjojen päivittämistä pidemmälle. Todellinen arvo on jatkuvassa innovoinnissa – uusissa rokotteissa, biologisissa lääkkeissä ja niitä tukevissa teknologioissa. Vain kattavan tutkimuksen ja strategisten investointien avulla prosessien kehittämiseen, viljelyalustoihin ja skaalautuviin järjestelmiin teollisuus voi saavuttaa globaalin kilpailukyvyn.
Johtopäätös
Suspensioviljelyteknologia on biolääketieteellisen innovaation eturintamassa. Se mahdollistaa rokotteiden ja terapeuttisten proteiinien tehokkaan, skaalautuvan ja yhdenmukaisen tuotannon. Alan kehittyessä edistyneiden soluviljelyalustojen integrointi personoituihin viljelyalustoihin ja älykkäisiin bioreaktorijärjestelmiin on avainasemassa biologisten lääkkeiden valmistuksen tulevaisuuden muokkaamisessa.