Le développement d’anticorps repose sur une approche Qualité par Conception (QbD) bien structurée pour la production en amont. En exploitant les avantages des plans d’expériences (DoE) et de la technologie des bioréacteurs parallèles à haut débit, les chercheurs peuvent mener à bien des processus de R&D à l’échelle du laboratoire. Une étape cruciale de ce processus est l’identification précoce de la relation entre les attributs critiques de qualité (CQA) et les paramètres critiques de procédé (CPP), ce qui permet de définir l’espace de conception pendant le développement.
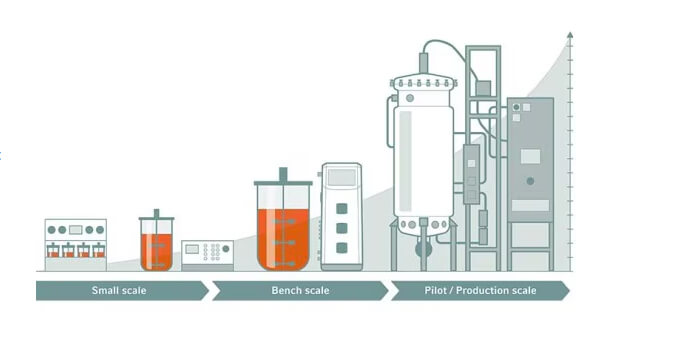
Une fois les processus de R&D à petite échelle mis en place avec succès, le défi suivant consiste à les déployer à l’échelle pilote et en production. Idéalement, un processus de mise à l’échelle efficace peut passer de la R&D à la production complète en 2 à 4 mois. Cependant, un transfert et une mise à l’échelle fluides des procédés nécessitent une expertise et une expérience approfondies de la part de toute l’équipe chargée des technologies des procédés.
Considérations clés pour la mise à l’échelle des processus
L’objectif principal de la mise à l’échelle du procédé est de maintenir un environnement cellulaire stable pour une expression constante du produit à mesure que le volume de culture augmente. Les principaux indicateurs d’évaluation de la mise à l’échelle du procédé sont les suivants :
- Densité cellulaire et taux de croissance
- Viabilité et productivité
- Taux d’expression du produit
- Profils de glycosylation
Lors de la mise à l’échelle, les paramètres clés de contrôle du processus peuvent être classés comme suit :
- Facteurs indépendants du volume, tels que la température, l’oxygène dissous (OD) et le pH.
- Facteurs dépendant du volume, tels que la vitesse d’agitation et le taux d’aération, qui sont influencés par la taille et la géométrie du récipient.
La R&D utilisant des bioréacteurs de différents fournisseurs, les différences de matériaux (jetables ou en verre), de rapports d’aspect, de conception des turbines et de géométrie des cuves compliquent le maintien de conditions d’agitation et d’aération constantes après la mise à l’échelle. Pour garantir un environnement de culture uniforme, les développeurs s’appuient sur les stratégies de mise à l’échelle suivantes :
Stratégies courantes de mise à l’échelle
1. Vitesse constante de la pointe de la lame
Les forces de cisaillement dues à l’agitation affectent significativement la viabilité cellulaire, les différentes lignées cellulaires présentant des tolérances variables. Les premières lignées cellulaires CHO étaient très sensibles aux contraintes de cisaillement, mais les lignées cellulaires modernes, issues de l’ingénierie génétique, présentent une plus grande résilience.
La vitesse de rotation des pales, déterminée par le diamètre de la turbine et la vitesse de rotation, est un facteur clé pour maintenir des forces de cisaillement constantes. Les bioréacteurs de plus grande taille nécessitant des turbines plus grandes, leur vitesse de rotation est réduite en conséquence afin de préserver des conditions de cisaillement similaires. Cette méthode est particulièrement efficace pour les petites et moyennes mises à l’échelle.
2. Temps de mélange constant
Le temps de mélange, paramètre critique en génie chimique, assure une distribution uniforme des nutriments et des gaz. Si les bioréacteurs de petite taille (par exemple, 2 L) permettent un mélange rapide, des volumes plus importants nécessitent des vitesses de rotation plus élevées, ce qui peut augmenter la contrainte de cisaillement et impacter la viabilité cellulaire. Par conséquent, cette stratégie est plus applicable aux procédés chimiques qu’à la culture cellulaire.
3. Coefficient de transfert d’oxygène constant (kLa)
Le coefficient de transfert volumétrique d’oxygène (kLa) détermine la disponibilité en oxygène, essentielle au métabolisme cellulaire. Le maintien d’un kLa constant assure un environnement de transfert d’oxygène uniforme à toutes les échelles. Cependant, ce coefficient est influencé par de multiples facteurs, notamment les taux d’agitation et d’aération, ce qui nécessite une optimisation poussée. À mesure que le volume du réacteur augmente, l’accumulation de CO2 devient un défi, ce qui complique encore davantage le maintien du kLa.
4. Puissance constante par unité de volume (P/V)
Le rapport P/V, fonction de l’indice de puissance de la turbine (Np), de la géométrie de la cuve et des propriétés du liquide, influence l’efficacité du mélange et du transfert de masse. Il est largement considéré comme le critère de mise à l’échelle le plus efficace et le plus couramment utilisé. Compte tenu des tolérances de cisaillement spécifiques à chaque lignée cellulaire, la plage P/V recommandée se situe généralement entre 10 et 40 W/m³.
Considérations supplémentaires sur la culture à grande échelle
Au-delà des critères primaires de mise à l’échelle, les bioréacteurs à plus grande échelle doivent tenir compte des effets de l’accumulation de CO₂ sur la croissance cellulaire et l’expression des protéines. Contrairement aux systèmes à petite échelle où les échanges gazeux éliminent naturellement le CO₂ métabolique, les cultures à grande échelle présentent une efficacité d’élimination du CO₂ réduite en raison de valeurs kLa CO₂ plus faibles. Des facteurs tels que la saturation en gaz et la dynamique des bulles doivent être gérés par des stratégies d’aération améliorées ou des systèmes intégrés d’élimination du CO₂.
S’adapter aux défis des processus en constante évolution
À mesure que la technologie des anticorps progresse, les défis liés à la mise à l’échelle des procédés continuent d’évoluer. Les développeurs de procédés doivent rester flexibles et adapter leurs stratégies de mise à l’échelle aux caractéristiques des lignées cellulaires et aux exigences spécifiques des produits. Une approche globale (équilibre entre P/V, vitesse de pointe de la lame, élimination du CO2 et kLa) garantit des performances optimales du procédé tout en préservant les critères de qualité essentiels.
En intégrant des principes avancés d’ingénierie des procédés, les entreprises biopharmaceutiques peuvent réaliser une mise à l’échelle fiable et efficace, facilitant ainsi la transition transparente de la R&D à la production à grande échelle.