Biologisten lääkkeiden tuotantoon tarkoitetun mikrobikäymisen kiinnostuksen viimeaikainen uudelleen herääminen voidaan selittää useilla keskeisillä tekijöillä. Erityisesti biokemian kehitys ja glykosylaatioprosessien syvempi ymmärtäminen ovat valaisseet tilanteita, joissa glykosylaatio ei välttämättä ole toivottavaa. Tämä kehittyvä tieto on tasoittanut tietä innovatiivisille lähestymistavoille biologisten lääkkeiden valmistuksessa. Uusien proteiinimuotojen ja -rakenteiden syntyminen, jotka sopivat saumattomasti yhteen mikrobien käymisteknologioiden kanssa, on entisestään vauhdittanut tätä trendiä. Nämä uudet rakenteet eivät ainoastaan paranna tuotannon tehokkuutta, vaan myös laajentavat mikrobijärjestelmien sovellettavuutta DNA-plasmidien tuotantoon. Onnistuneiden optimointitoimien avulla on nyt mahdollista kehittää skaalautuvia käymisprosesseja, jotka saavuttavat paitsi korkeat titterit ja tuottavuuden, myös huomattavan stabiilisuuden ja luotettavuuden.
Oikeissa olosuhteissa tämä lähestymistapa tarjoaa erittäin houkuttelevan vaihtoehdon biologisten lääkkeiden tuotantoon. Useita haasteita on kuitenkin vielä ratkottava. Bakteereilta ja hiivoilta puuttuu tyypillisesti solukoneisto, jota tarvitaan monimutkaisten biologisten rakenteiden prosessointiin. Tämä rajoitus korostaa sopivimman tuotantojärjestelmän valinnan kriittistä merkitystä kullekin kohdemolekyylille. Lisäksi merkittävä este on ilmentämisjärjestelmien ja -prosessien riittämätön ymmärtäminen, mikä vaikeuttaa sekä määrä- että laatuvaatimukset täyttävien proteiinien tuotantoa. Onneksi alan jatkaessa herkempien teknologioiden käyttöönottoa on nyt ennennäkemätön tilaisuus saada tietoa tuotteen laadusta kehitysvaiheen aiemmissa vaiheissa. Tämä edistysaskel mahdollistaa perusteellisemman ymmärryksen siitä, miten halutut laatuominaisuudet saavutetaan alusta alkaen. Se edellyttää kuitenkin myös useampia iteraatioita kehitysvaiheen aikana, jotta varmistetaan, että nämä laatukriteerit täyttyvät prosessin alkuvaiheessa.
Mikrobifermentaation skaalaaminen tuo mukanaan useita haasteita, erityisesti prosessinohjauksen, hapensiirron ja lämmönhallinnan osalta. Nämä tekijät ovat ratkaisevan tärkeitä kasvuolosuhteiden optimoinnille, erityisesti nopeasti kasvaville bakteeriviljelmille. Kasvunopeuksien maksimoimiseksi on tärkeää varmistaa riittävä hapen kuljetus koko viljelyjärjestelmässä. Tämä vaatimus edellyttää tehokasta sekoittamista ja sopivaa ilmavirran nopeutta. Riittämätön happi voi haitata mikrobien aineenvaihduntaa, mikä lopulta vaikuttaa saantoon ja tuottavuuteen. Lämmönhallinta on toinen kriittinen osa mikrobifermentaatiota. Toisin kuin soluviljelmät, mikrobifermentaatio tuottaa enemmän lämpöä, mikä edellyttää tarkkaa lämpötilan säätöä, tyypillisesti ±1 tai 2 °C:n tarkkuudella. Laitteiden on poistettava ylimääräinen lämpö tehokkaasti, jotta estetään hallitsemattomat lämpötilapiikit, jotka voivat aiheuttaa merkittäviä haasteita laajamittaisessa tuotannossa.
Antibioottien käyttö sellaisten bakteerien valitsemiseksi, jotka kykenevät ylläpitämään halutun tuotteen korkeita ilmentymistasoja, tuo ainutlaatuisen haasteen bakteerikäymiseen. Käsittelyn jälkeen on välttämätöntä poistaa nämä antibiootit, koska sääntelyelimet odottavat valmistajien osoittavan tehokkaan eliminointinsa. Tämä saavutetaan usein käyttämällä hyvin alhaisia alkupitoisuuksia spesifisiä antibiootteja ja varmistamalla niiden poistaminen kohdennetuilla analyyttisillä menetelmillä. Lisäksi eri puhdistusvaiheiden aikana havaitut laimennusvaikutukset voivat auttaa tässä prosessissa. Näihin haasteisiin vastauksena isäntäjärjestelmien kehittäminen, jotka eivät ole riippuvaisia antibiooteista ja jotka varmistavat vakaan ilmentymisen, on tullut tärkeäksi tavoitteeksi rekombinanttiproteiinien ja plasmidien tuotannossa. Tämä innovaatio ei ainoastaan paranna sääntelystandardien noudattamista, vaan myös virtaviivaistaa tuotantoprosessia. Plasmidituotannon lisääminen on toinen haaste; pelkkä solujen määrän lisääminen ei takaa korkeampia plasmidisantoja. Plasmidien säilyttäminen voi vaikuttaa haitallisesti solujen kasvuun, mikä edellyttää huolellista tasapainoa plasmidisaannon optimoinnin ja riittävän kasvunopeuden ylläpitämisen välillä. Tämän tasapainon saavuttaminen voi olla monimutkaista ja vaatii harkittuja optimointistrategioita.
Yksi merkittävä ominaisuus, joka vaikuttaa mikrobifermentaation soveltuvuuteen biolääketuotantoon, on tiettyjen mikro-organismien glykosylaatiokyky. Esimerkiksi Escherichia coli (E. coli) pystyy rajoitetusti suorittamaan translaation jälkeisiä modifikaatioita, kun taas hiivalla on kyky glykosyloida proteiineja, vaikkakaan ei samalla tavalla kuin nisäkässoluilla. Vaadittavien translaation jälkeisten modifikaatioiden luonne sanelee lopulta isäntäorganismin valinnan tuotantoa varten. Vaikka joitakin modifikaatioita voidaan saavuttaa in vitro -tekniikoilla, isäntäorganismin solukoneiston hyödyntäminen on yleensä parempi vaihtoehto. Tämä lähestymistapa mahdollistaa biologisten lääkkeiden luonnollisemman ja tehokkaamman tuotannon. Vaikka prosessiparametrien optimointi voi parantaa tuloksia, se ei voi täysin korvata valitun mikro-organismin luontaisia ominaisuuksia. Näin ollen E. coli ja hiiva osoittautuvat tehokkaiksi ja toisiaan täydentäviksi järjestelmiksi biomolekyylien tuottamiseen, jotka eivät vaadi ihmisen kaltaista glykosylaatiota.
Käymisprosessien alalla tuotantoparametrien reaaliaikainen seuranta on tullut olennaiseksi tehtäväksi biolääketeollisuudelle. Prosessianalyysiteknologian (PAT) integrointi käymisen aikana mahdollistaa mahdollisesti ongelmallisten muutosten tunnistamisen reaaliajassa. Tämä ominaisuus helpottaa joko manuaalisia tai automatisoituja säätöjä prosessin pitämiseksi todistetusti toimivalla alueella. Käyttämällä PAT:ta valmistajat voivat parantaa sekä käymisprosessiensa onnistumista että johdonmukaisuutta. Tämä ennakoiva lähestymistapa ei ainoastaan säästä aikaa ja resursseja, vaan myös ylläpitää korkeimpia laatustandardeja koko tuotannon ajan.
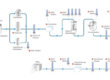
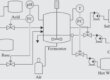
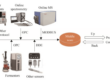
Mikrobifermentaation optimointi proteiinin tuotantoa varten edellyttää käytettävän organismin tyypin huolellista harkintaa. Tietyissä prosessimalleissa isäntäorganismi voi erittää proteiinin tehokkaasti fermentaatioalustaan, mikä helpottaa suhteellisen suoraviivaista uuttamista tangentiaalisen virtaussuodatuksen (TFF) avulla onttoja kuitukalvoja käyttäen. Sitä vastoin muut prosessit, kuten Escherichia coli (E. coli) -bakteeriin liittyvät, tuottavat proteiineja sytoplasmassa joko liukoisina proteiineina tai liukenemattomina inkluusiokappaleina. Nämä vaihtelevat tuotantomenetelmät vaativat räätälöityjä keräysstrategioita, jotka ovat spesifisiä tuotetulle tuotteelle. Sytoplasmaan jääneet proteiinit edellyttävät täydellistä solujen hajoamista, joka voidaan saavuttaa mekaanisilla menetelmillä, kuten korkeapainehomogenisaatiolla. Tämä lähestymistapa rikkoo solut tehokkaasti, jolloin halutut proteiinit vapautuvat ympäröivään alustaan. Sitä vastoin liukenemattomina inkluusiokappaleina tuotetut proteiinit vaativat lisätoimenpiteitä niiden avaamiseksi ja uudelleenlaskostamiseksi, jotta saadaan liukoisia, oikein laskostuneita tuotteita. Nämä ylimääräiset vaiheet eivät ainoastaan monimutkaista koko prosessia, vaan myös lisäävät kontaminaatioriskiä tai mahdollista vaurioitumista lopputuotteelle.
Liukenemattomina inkluusiokappaleina tuotetut proteiinit sitä vastoin vaativat monimutkaisia purkamis- ja uudelleenlaskostusmenetelmiä liukoisten, oikein laskostuneiden tuotteiden saamiseksi. Nämä lisävaiheet eivät ainoastaan monimutkaista koko prosessia, vaan myös voivat aiheuttaa epäpuhtauksien pääsyn järjestelmään tai vahingoittaa lopputuotetta.
Solulinjojen muokkaus nousee lupaavaksi strategiaksi näiden haasteiden ratkaisemiseksi keskittymällä oikein laskostuneiden molekyylien muodostumisen tehostamiseen soluissa. Tämä lähestymistapa vaatii kuitenkin räätälöityä menetelmää kullekin tietylle tuotteelle, mikä vie merkittävästi aikaa ja vaivaa sopivan isännän valinnassa ja alkuperäisten prosessien kehittämisessä. Optimaalisten tiitterien ja saantojen saavuttamiseksi on ratkaisevan tärkeää valita huolellisesti sopivin organismi, ilmentämisjärjestelmä, toimintajärjestys ja olosuhteet heti projektin alusta alkaen.
Fermentointiprosessien monimuotoisuus ja niiden tuottamat erilaiset molekyylit vaikeuttavat universaalien mikrobien fermentointialustojen luomista. Monipuolisen solulinjan ja plasmidialustan kehittäminen, jota voidaan tehokkaasti hyödyntää tietyntyyppisille proteiineille tai tuotteille, olisi merkittävä edistysaskel fermentoinnin merkittävien haasteiden ratkaisemisessa. Lisäksi alustapohjaisen lähestymistavan käyttöönotto myöhemmissä prosessointivaiheissa voisi auttaa standardoimaan tiettyjä näiden tuotantoprosessien osa-alueita. Vaikka plasmidi-DNA:n tuotantoa varten tarkoitetut alustaratkaisut ovat saamassa jalansijaa, nämä lähestymistavat vaativat edelleen joustavuutta erilaisten plasmidien ja formaattien mukauttamiseksi.
Toinen tärkeä painopistealue mikrobikäymisen alalla on kaikkien osapuolten välinen johdonmukaisuus. Viranomaiset ovat laatineet selkeät ohjeet tiukkojen laatuvaatimusten mukaisten käymisprosessien kehittämiseksi. Tähän sisältyy järjestelmän ja sen toiminnallisuuden kattava ymmärtäminen sekä käymisen suunnittelutilan tunnistaminen.
Systemaattinen lähestymistapa on välttämätön fermentointiprosessien suunnittelussa ja optimoinnissa. Tämä edellyttää kokeellisen tutkimuksen tekemistä solulinjojen ja viljelyolosuhteiden välisten vuorovaikutusten sekä niiden vaikutuksen tuotteen kasvuun ja saantoon selvittämiseksi. Suuri osa prosessien kehittämiseen ja karakterisointiin liittyvästä työstä voidaan mallintaa tehokkaasti käyttämällä pieniä fermentoijia laboratorioympäristöissä.
Laboratoriomallien yhdenmukaistaminen valmistuksessa käytettyjen mallien kanssa on ratkaisevan tärkeää prosessien hienosäätöä ja luotettavan suorituskyvyn varmistamista varten laajassa mittakaavassa. Yhdenmukaisuuden ylläpitäminen eri parametrien välillä voi kuitenkin osoittautua haastavaksi, erityisesti kriittisten tekijöiden, kuten liuenneen hapen pitoisuuden, osalta. Siksi käytetyn säiliön tyypin huolellinen harkinta on elintärkeää mallien välisen yhdenmukaisuuden optimoimiseksi.
Pienen ja suuren mittakaavan mallien yhdistäminen mahdollistaa tutkijoiden tutkia poikkeamia normaaleista olosuhteista, mikä nopeuttaa prosessin johdonmukaisuuden ja vaihtelun analysointia ja samalla vähentää kustannuksia. Laboratoriomallit ovat arvokkaita työkaluja raaka-aineiden tunnistamiseen ja vaihtelun riskin arviointiin tuotantosyklien aikana.
On tärkeää huomata, että käymisreaktioiden optimoinnin ei tulisi keskittyä pelkästään saantoon; prosessin luotettavuus, tasaisuus ja muut kriittiset ominaisuudet – kuten happitasot ja hapen kuljetus – ovat yhtä tärkeitä. Käymisprosessin suunnittelussa tulisi ottaa huomioon odotetut tavoitetuotot ja käymisen lopulliset tavoitteet skaalautuvuusongelmien välttämiseksi.